Neue RSV-Prävention bei Kindern
Infektionen durch das Respiratorische Synzytial-Virus (RSV) sind eine der häufigsten Ursachen für Krankenhausaufenthalte und Todesfälle im frühen Kindesalter. Bei der Vorbeugung von Atemwegserkrankungen, die durch RSV ausgelöst werden, zeichnet sich nun ein bedeutender Fortschritt ab. Gleich mehrere Kandidaten für neue monoklonale Antikörper und Impfstoffe stehen kurz vor der Zulassung oder sind jüngst bereits zugelassen worden. Insbesondere für Säuglinge werden weitere Präventionsmöglichkeiten dringend erwartet. Als Präventivtherapie steht bisher lediglich ein monoklonaler Antikörper von Astrazeneca zur Verfügung (Handelsname Synagis). Er muss mehrfach gespritzt werden und ist auch nur für Risikokinder empfohlen [1] [2]. Einen Aktiv-Impfstoff gab es bislang nicht.
In diesem Fact Sheet werden die zwei vielversprechendsten neuen Präventionsangebote für Kinder näher betrachtet. Dabei handelt es sich um den jüngst zugelassenen monoklonalen Antikörper Beyfortus (Astrazeneca/Sanofi) und den Schwangeren-Impfstoff RSVpreF (Pfizer). Ein Entscheid der US-Arzneimittelbehörde FDA zu RSVpreF bei Schwangeren wird für August erwartet. Eine EU-Zulassung steht ebenfalls noch aus. Die aktive Impfung ist für Schwangere vorgesehen, die den Antikörperschutz im Mutterleib und später über das Stillen passiv an das Kind weitergeben [3].
Impfstoffe und monoklonale Antikörper sind Prophylaktika, unterscheiden sich jedoch in ihrer Funktionsweise: Während Impfstoffe das Immunsystem stimulieren, um eine spezifische Immunantwort gegen einen Erreger zu erzeugen, blockieren biomedizinisch hergestellte Antikörper direkt den Erreger. Monoklonale Antikörper sind meist teurer als Aktiv-Impfstoffe und vermitteln naturgemäß nur vorübergehenden Schutz. Pfizer und Astrazenca/Sanofi dringen darauf, ihre Arzneien schon vor der kommenden RSV-Saison auf den Markt bringen zu können.
Daneben stehen auch aussichtsreiche Kandidaten für eine Immunisierung von Erwachsenen bereit. So ist der Impfstoff von Pfizer auch für Ältere vorgesehen – und als solcher nun unter dem Handelsnamen Abrysvo in den USA zugelassen [4]. Die Firma Glaxo-Smith-Kline (GSK) hat ebenfalls einen derartigen Impfstoff entwickelt (Handelsname Arexvy). Er ist in den USA und der EU seit Kurzem zugelassen und soll bald verfügbar sein [5] [6].
Die Entwicklung einer RSV-Prophylaxe stockte über mehrere Jahrzehnte. Ein Misserfolg in den 60er-Jahren warf die gesamte Forschung zurück: Nach dem Vorbild des ersten Polio-Impfstoffs stellten Forschende einen experimentellen RSV-Impfstoff her, indem sie das Virus in einem Labor züchteten und es abtöteten. Tests an Kindern ergaben jedoch nicht nur eine unbefriedigende Schutzwirkung, bei geimpften Kindern mit anschließender RSV-Infektion kam es sogar zu schweren Verläufen mit zwei Todesfällen.
Dieses Fact Sheet kann hier als pdf heruntergeladen werden.
Übersicht
- Beyfortus (Astrazeneca/Sanofi)
- RSVpreF (Pfizer)
- Weitere präventive RSV-Arzneien für Kinder
- Fazit
- Literaturstellen, die zitiert wurden
Beyfortus (Astrazeneca/Sanofi)
Wirksamkeit
- monoklonaler Antikörper, hemmt den entscheidenden Membranfusionsschritt beim Viruseintritt in die Zelle und neutralisiert das Virus
- Zulassungsstudie umfasste 1490 Säuglinge; 994 Beyfortus-Gruppe, 496 Placebo-Gruppe [7]
- medizinisch betreute RSV-bedingte Infektionen der unteren Atemwege traten 150 Tage nach Injektion bei 12 Säuglingen (1,2 Prozent) in der Beyfortus-Gruppe und bei 25 Säuglingen (5,0) in der Placebo-Gruppe auf
- entspricht einer Wirksamkeit gegen RSV-bedingte Atemwegserkrankungen von 74,5 Prozent
- die Wirksamkeit ergibt sich bei derlei Studien aus dem Vergleich der Anteile der Krankheitsfälle in beiden Untersuchungsgruppen
- innerhalb von 150 Tagen wurden 6 Säuglinge (0,6 Prozent) in der Beyfortus-Gruppe und 8 Säuglinge (1,6) in der Placebo-Gruppe ins Krankenhaus eingeliefert
- entspricht einer Wirksamkeit gegen RSV-bedingte Hospitalisierung von 62,1 Prozent
Schutz vor Erkrankung und Hospitalisierung
„Ärztlich behandelte Infektionen der unteren Atemwege und Krankenhausaufenthalte im Zusammenhang mit dem Respiratory Syncytial Virus (RSV) bis 150 Tage nach der Injektion“

Mögliche Nebenwirkungen
- monoklonale RSV-Antikörper haben traditionell ein gutes Sicherheitsprofil und viele „unerwünschte Ereignisse“ (AEs) sind de facto Symptome der zu verhindernden Erkrankung oder Folge der Applikation
- dementsprechend kam es in beiden Gruppen ähnlich häufig zu „unerwünschten Ereignissen“ wie kurzzeitigem Hautausschlag/Schwellungen: 863 Säuglinge (87,4 Prozent) in der Beyfortus-Gruppe und 426 (86,8) in der Placebo-Gruppe
- in klinischen Studien sind AEs alle unerwünschten medizinischen Ereignisse bei Probanden, denen ein Arzneimittel verabreicht wurde; sie stehen nicht automatisch in einem kausalen Zusammenhang zur Behandlung
- „schwerwiegende unerwünschte Ereignisse“ (SAE) traten bei 67 Säuglingen (6,8) beziehungsweise 36 (7,3) in der Placebo-Gruppe auf
- als „schwerwiegend“ gelten in klinischen Studien mögliche lebensbedrohliche Nebenwirkungen oder solche, die zu einem Krankenhausaufenthalt führen
- in der Impfstoff-Gruppe starben drei Säuglinge (0,3 Prozent), in der Placebo-Gruppe keiner
- keines der „schwerwiegenden unerwünschten Ereignisse“, einschließlich der Todesfälle, wurde von den Prüfärzten ursächlich mit dem Impfstoff oder dem Placebo in Verbindung gebracht
Verabreichung
- aufgrund der langen Verweildauer im Organismus reicht eine einmalige Verabreichung: 50-mg-Einmaldosis als Injektion in den Oberschenkelmuskel bei Säuglingen unter fünf Kilogramm; 100-mg-Einmaldosis bei über fünf Kilogramm [8]
- Ausnahme: Bei Kindern mit Operationen unter Herz-Lungen-Maschine ist eine zweite Dosis zu erwägen
- Anwendung vor Beginn der RSV-Saison oder ab der Geburt bei Säuglingen/Kleinkindern, die während der RSV-Saison geboren werden
- zugelassen als Injektion, um Säuglinge und Kleinkinder vor RSV zu schützen
RSVpreF (Pfizer)
Wirksamkeit
- Impfstoff, enthält als Antigen das preF-Glykoprotein der RSV-A- und -B-Stämme
- Zulassungsstudie mit 7358 schwangeren Frauen; 3682 in der RSVpreF-Gruppe, 3676 in der Placebo-Gruppe [9]
- insgesamt wurden 3570 Säuglinge von Müttern, die den RSVpreF-Impfstoff erhalten hatten, und 3558 von Müttern, die ein Placebo erhalten hatten, geboren
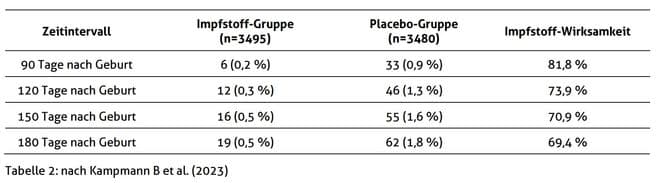
- schwere RSV-bedingte Atemwegserkrankungen traten innerhalb von 90 Tagen nach der Geburt bei 6 Säuglingen in der Impfstoff-Gruppe und bei 33 Säuglingen in der Placebo-Gruppe auf
- entspricht einer Impfstoff-Wirksamkeit von 81,8 Prozent
- bei allen RSV-bedingten Atemwegserkrankungen, also auch leichten, lag die Wirksamkeit nach 90 Tagen lediglich bei 57,1 Prozent; diese Ergebnisse erfüllten nicht das statistische Erfolgskriterium der Studie
- da es sich um eine passive Immunität handelt, war jedoch zu erwarten, dass die Schutzwirkung im Laufe der Monate nach der maternalen Impfung abnimmt
Schutz vor schweren RSV-Erkrankungen
„Ärztlich behandelte schwere RSV-assoziierte Erkrankung der unteren Atemwege“
Schutz vor allen RSV-Erkrankungen
„Medizinisch betreute RSV-assoziierte Erkrankung der unteren Atemwege“

Mögliche Nebenwirkungen
- die meisten Reaktionen auf den Impfstoff oder das Placebo waren leicht bis mittelschwer
- lokale Reaktionen traten erwartungsgemäß bei RSVpreF-Impflingen häufiger auf als beim Placebo; am häufigsten waren Schmerzen an der Injektionsstelle
Mütter
- systemische „unerwünschte Ereignisse“ (AE) traten bei 13,8 Prozent der Schwangeren in der Impfstoff-Gruppe und bei 13,1 Prozent in der Placebo-Gruppe auf
- „schwerwiegende unerwünschte Ereignisse“ (SAE) traten bei 4,2 Prozent der geimpften Mütter auf, 3,7 Prozent in der Placebo-Gruppe
- fünf Fälle standen den Prüfärzten zufolge mit der Injektion im Zusammenhang: Schmerzen in Armen und Beinen; vorzeitige Wehen; systemischer Lupus erythematodes und Eklampsie (alles Impfstoff-Gruppe) sowie vorzeitige Ablösung der Plazenta (Placebo-Gruppe)
Säuglinge
- bei den Säuglingen lag der AE-Anteil kurz nach Geburt bei 37,1 beziehungsweise 34,5 Prozent
- der SAE-Anteil lag bei 15,5 beziehungsweise 15,2 Prozent
- keines der „schwerwiegenden unerwünschten Ereignisse“ bei den Säuglingen wurde von den Prüfärzten mit dem Impfstoff oder dem Placebo in Verbindung gebracht
Frühgeburten
- Pfizer-Konkurrent GSK stoppte vergangenes Jahr Studien mit Schwangeren, nachdem dort ein Sicherheitssignal bei Frühgeburten auftrat: die Wahrscheinlichkeit einer Frühgeburt war bei geimpften Schwangeren um 38 Prozent höher als in der Placebo-Gruppe [10] [11]
- erhöhte Inzidenz auch in der RSVpreF-Studie: 202 Frühgeburten (5,7 Prozent) zu 169 (4,7); prozentualer Unterschied: 21,3 Prozent [9]
- durchschnittliche Inzidenz von Frühgeburten (vor der 37. Schwangerschaftswoche) liegt laut WHO bei rund 10 Prozent, schwankt je nach Land aber stark [12]
- demnach wären bei 3568 Schwangeren in der Impfstoff-Gruppe rein statistisch betrachtet mehr Frühgeburten zu erwarten gewesen: rund 356
- in Deutschland ebenso: hier liegt die Frühgeburtenrate bei etwa 8 Prozent [13]; demnach wären rund 285 Frühgeburten zu erwarten gewesen
- kleine Stichprobe in der RSVpreF-Studie lässt keine qualifizierte Aussage zur Zahl der Frühgeburten zu; andere Impfstoffe (Grippe, Tetanus, Keuchhusten), die auch Schwangere erhalten können und breit verimpft werden, weisen kein entsprechendes Sicherheitssignal auf
Verabreichung
- bei Schwangeren Einmalimpfung in den Oberarm (24. bis 34. Schwangerschaftswoche)
- Einmaldosis 120 μg RSVpreF
Weitere präventive RSV-Arzneien für Kinder
Clesrovimab
- monoklonaler Antikörper von Merck für gesunde Säuglinge
- Phase-III-Studie läuft, Fertigstellungstermin voraussichtlich August 2025 [14]
mRNA-1345
- mRNA-Impfstoff von Moderna
- Phase-III-Studie an Erwachsenen durchgeführt, Phase-I für Kinder gestartet [15]
Fazit
- bisherige RSV-Prophylaxe mit Synagis wichtig, aber aufwendig und nur für Risikokinder
- mit neuen Präventionsstrategien zeichnet sich eine breitere Lösung für das Public-Health-Problem „RSV“ ab
- Synagis wird weiterhin insbesondere für Frühgeborene zur Verfügung stehen
- Beyfortus ermöglicht einfachen Schutz vieler anderer Säuglinge und Kleinkinder
- RSV-Impfung der Schwangeren mit RSVpreF ist ein weiteres vielversprechendes Prophylaktikum; ein mögliches Sicherheitssignal bei Frühgeburten muss weiter evaluiert werden, erscheint bisher jedoch nicht sehr wahrscheinlich
Literaturstellen, die zitiert wurden
[1] Deutsche Gesellschaft für Pädiatrische Infektiologie (2018): S2k-Leitlinie zur Prophylaxe von schweren Erkrankungen durch Respiratory Syncytial Virus (RSV) bei Risikokindern Aktualisierung 2017/2018.
[2] Europäische Arzneimittel-Agentur (2023): Produktinformation Synagis.
[3] Pfizer (01.11.2022): Pfizer Announces Positive Top-Line Data of Phase 3 Global Maternal Immunization Trial for its Bivalent Respiratory Syncytial Virus (RSV) Vaccine Candidate. Pressemitteilung.
[4] Pfizer (31.05.2023): U.S. FDA Approves ABRYSVO™, Pfizer’s Vaccine for the Prevention of Respiratory Syncytial Virus (RSV) in Older Adults. Pressemitteilung.
[5] U.S. Food & Drug Administration (03.05.2023): FDA Approves First Respiratory Syncytial Virus (RSV) Vaccine. Pressemitteilung.
[6] Europäische Arzneimittel-Agentur (26.04.2023): First vaccine to protect older adults from respiratory syncytial virus (RSV) infection. Pressemitteilung.
[7] Hammitt LL et al. (2023): Nirsevimab for Prevention of RSV in Healthy Late-Preterm and Term Infants. The New England Journal of Medicine. DOI: 10.1056/NEJMoa2110275.
[8] Europäische Arzneimittel-Agentur (2023): Produktinformation Beyfortus.
[9] Kampmann B et al. (2023): Bivalent Prefusion F Vaccine in Pregnancy to Prevent RSV Illness in Infants. The New England Journal of Medicine. DOI: 10.1056/NEJMoa2216480.
[10] Glaxo-Smith-Kline (22.02.2022): GSK provides further update on phase III RSV maternal vaccine candidate programme. Pressemitteilung.
[11] U.S. Food & Drug Administration (28.03.2023): RSVPreF Sponsor Briefing Document. Vaccines and related biological Advisory Commitee.
[12] Word Health Organization (10.05.2023): Preterm birth. Fact sheet.
[13] Institut für Qualitätssicherung und Transparenz im Gesundheitswesen (10.08.2021): Bundesauswertung zum Erfassungsjahr 2020. Geburtshilfe. Qualitätsindikatoren und Kennzahlen.
[14] Merck (2023): Clesrovimab in Infants and Children at Increased Risk for Severe Respiratory Syncytial Virus Disease. Clinical Trial.
[15] Moderna (17.01.2023): Moderna Announces mRNA-1345 an Investigational Respiratory Syncytial-Virus-RSV-Vaccine Has Met Primary Efficacy Endpoints in Phase-3-Trial in Older Adults. Pressemitteilung.

